Хвильова природа електрона
Фізика атома і атомного ядра
Поняття атомів як неподільних найдрібніших частинках речовини виникло ще в античні часи, але тільки в XVIII столітті працями А. Лавуазьє, М. В. Ломоносова та інших вчених була доведена реальність існування атомів. Питання про їх внутрішній устрій навіть не виникало, і атоми як і раніше вважалися неподільними частками. У XIX столітті вивчення атомістичного будови речовини істотно просунулося вперед. У 1833 році при дослідженні явища електролізу М. Фарадей встановив, що струм у розчині електроліту це впорядкований рух заряджених частинок - іонів. Фарадей визначив мінімальний заряд іона, який був названий елементарним електричним зарядом. Його наближене значення виявилося рівним e = 1,60 • 10-19 Кл.
На підставі досліджень Фарадея можна було зробити висновок про існування всередині атомів електричних зарядів.
Велику роль у розвитку атомістичної теорії відіграв видатний російський хімік Д. І. Менделєєв, який розробив в 1869 році періодичну систему елементів, в якій вперше було поставлено питання про єдину природу атомів. Важливим свідченням складної структури атомів з'явилися спектроскопічні дослідження, які привели до відкриття лінійчатих спектрів атомів. На початку XIX століття були відкриті дискретні спектральні лінії у випромінюванні атомів водню у видимій частині спектру. Згодом, у 1885 р. І. Бальмером були встановлені математичні закономірності, що зв'язують довжини хвиль цих ліній.
У 1896 році А. Беккерель виявив явище випускання атомами невидимих проникаючих випромінювань, назване радіоактивністю. У наступні роки явище радіоактивності вивчалося багатьма вченими (М. Склодовська-Кюрі, П. Кюрі, Е. Резерфорд та ін.) Було виявлено, що атоми радіоактивних речовин випускають три види випромінювань різної фізичної природи (альфа-, бета-і гамма-промені). Альфа-промені виявилися потоком іонів гелію, бета-промені - потоком електронів, а гамма-промені - потоком квантів жорсткого рентгенівського випромінювання.
У 1897 році Дж. Томсон відкрив електрон і виміряв ставлення e / m заряду електрона до маси. Досліди Томсона підтвердили висновок про те, що електрони входять до складу атомів.
Таким чином, на підставі всіх відомих до початку XX століття експериментальних фактів можна було зробити висновок про те, що атоми речовини мають складну внутрішню будову. Вони являють собою електронейтральні системи, причому носіями негативного заряду атомів є легкі електрони, маса яких становить лише малу частку маси атомів. Основна частина маси атомів пов'язана з позитивним зарядом.
Перед наукою постало питання про внутрішню будову атомів.
Досвід Резерфорда. Ядерна модель атома
Перша спроба створення моделі атома на основі накопичених експериментальних даних (1903 р.) належить Дж. Томсону. Він вважав, що атом є електронейтральної систему кулястої форми радіусом, приблизно рівним 10-10 м. Позитивний заряд атома рівномірно розподілений по всьому об'єму кулі, а негативно заряджені електрони знаходяться всередині нього (рис. 6.1.1). Для пояснення лінійчатих спектрів випускання атомів Томсон намагався визначити розташування електронів в атомі і розрахувати частоти їх коливань близько положень рівноваги. Проте ці спроби не увінчалися успіхом.Через кілька років у дослідах великого англійського фізика Е. Резерфорда було доведено, що модель Томсона невірна.
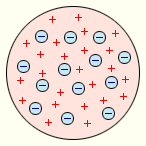
Модель атома Дж. Томсона
Перші прямі експерименти з дослідження внутрішньої структури атомів були виконані Е. Резерфордом і його співробітниками Е. Марсденом і Х. Гейгером у 1909-1911 роках. Резерфорд запропонував застосувати зондування атома за допомогою α-частинок, які виникають при радіоактивному розпаді радію і деяких інших елементів. Маса α-частинок приблизно в 7300 разів більше маси електрона, а позитивний заряд дорівнює подвоєному елементарному заряду. У своїх дослідах Резерфорд використовував α-частинки з кінетичною енергією близько 5 МеВ (швидкість таких частинок дуже велика - близько 107 м / с, але все ж таки значно менше швидкості світла). α-частинки - це повністю іонізовані атоми гелію. Вони були відкриті Резерфордом у 1899 році при вивченні явища радіоактивності. Цими частками Резерфорд бомбардував атоми важких елементів (золото, срібло, мідь та ін.)Електрони, що входять до складу атомів, внаслідок малої маси не можуть помітно змінити траєкторію α-частинки. Розсіювання, тобто зміна напрямку руху α-частинок, може викликати лише важка позитивно заряджена частина атома.
Схема досліду Резерфорда
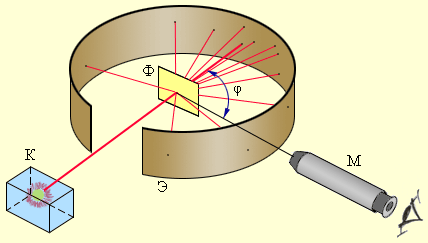
Схема досліду Резерфорда по розсіюванню α-частинок. K - свинцевий контейнер з радіоактивною речовиною, Е - екран, покритий сірчистим цинком, Ф - золота фольга, M - мікроскоп
Від радіоактивного джерела, укладеного в свинцевий контейнер, α-частинки спрямовувалися на тонку металеву фольгу. Розсіяні частки потрапляли на екран, покритий шаром кристалів сульфіду цинку, здатних світитися під ударами швидких заряджених частинок.Сцинтиляції (спалаху) на екрані спостерігалися оком за допомогою мікроскопа. Спостереження розсіяних α-частинок в досвіді Резерфорда можна було проводити під різними кутами φ до первісного напрямку пучка. Було виявлено, що більшість α-частинок проходить через тонкий шар металу, практично не відчуваючи відхилення. Однак невелика частина часток відхиляється на значні кути, що перевищують 30 °. Дуже рідкісні α-частинки (приблизно одна на десять тисяч) зазнавали відхилення на кути, близькі до 180 °.
Цей результат був цілком несподіваним навіть для Резерфорда. Його уявлення в різкому протиріччі з моделлю атома Томсона, згідно якій позитивний заряд розподілений по всьому обсязі атома.При такому розподілі позитивний заряд не може створити сильне електричне поле, здатне відкинути α-частинки тому. Електричне поле однорідного зарядженого кулі максимально на його поверхні і убуває до нуля в міру наближення до центру кулі. Якби радіус кулі, в якому зосереджений весь позитивний заряд атома, зменшився в n разів, то максимальна сила відштовхування, що діє на α-частинку, за законом Кулона зросла б у n2 разів. Отже, при досить великому значенні n α-частинки могли б випробувати розсіювання на великі кути аж до 180 °.Ці міркування привели Резерфорда до висновку, що атом майже порожній, і весь його позитивний заряд зосереджений в малому обсязі.Цю частину атома Резерфорд назвав атомним ядром. Так виникла ядерна модель атома. Рис. 6.1.3 ілюструє розсіювання α-частинки в атомі Томсона і в атомі Резерфорда.
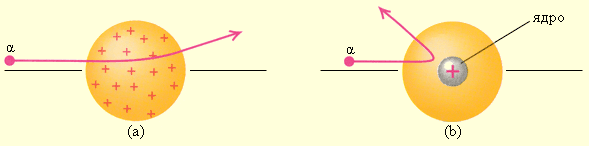
α-частинки в атомі Томсона (a) і в атомі Резерфорда (b).
Таким чином, досліди Резерфорда і його співробітників привели до висновку, що в центрі атома знаходиться щільне позитивно заряджене ядро, діаметр якого не перевищує 10-14-10-15 м. Це ядро займає лише 10-12 частина повного об'єму атома, але містить весь позитивний заряд і не менш 99,95% його маси. Речовині, що становить ядро атома, слід було приписати колосальну щільність порядку ρ ≈ 1015 г/см3. Заряд ядра повинен бути дорівнює сумарному заряду всіх електронів, що входять до складу атома. Згодом вдалося встановити, що якщо заряд електрона прийняти за одиницю, то заряд ядра в точності дорівнює номеру цього елемента в таблиці Менделєєва. Радикальні висновки про будову атома, що слідували з дослідів Резерфорда, змушували багатьох вчених сумніватися в їх справедливості. Не був винятком і сам Резерфорд, який опублікував результати своїх досліджень тільки в 1911 р. через два роки після виконання перших експериментів. Спираючись на класичні уявлення про рух мікрочастинок, Резерфорд запропонував планетарну модель атома. Відповідно до цієї моделі, в центрі атома розташовується позитивно заряджене ядро, в якому зосереджена майже вся маса атома. Атом в цілому нейтральний. Навколо ядра, подібно планет, під дією кулонівських сил з боку ядра обертаються електрони.Перебувати в стані спокою електрони не можуть, так як вони впали б на ядро.
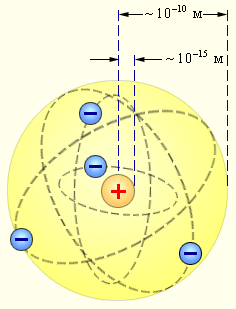
Планетарна модель атома Резерфорда. Показані кругові орбіти чотирьох електронів
Планетарна модель атома, запропонована Резерфордом, безсумнівно стала великим кроком вперед у розвитку знань про будову атома. Вона була абсолютно необхідною для пояснення дослідів з розсіювання α-частинок, проте виявилася нездатною пояснити сам факт тривалого існування атома, тобто його стійкість. За законами класичної електродинаміки, який рухається з прискоренням заряд повинен випромінювати електромагнітні хвилі, що забирають енергію. За короткий час (порядку 10-8 с) всі електрони в атомі Резерфорда повинні розтратити усю свою енергію і впасти на ядро.Те, що цього не відбувається в стійких станах атома, показує, що внутрішні процеси в атомі не підкоряються класичними законами.
Оцініть новину: 



