Статті / Мої статті
Практична робота: 3. Добування кисню в лабораторії та вивчення його властивостей
Склади прилад, як показано на мал. 79, і перевір його на герметичність (мал. 80). У суху пробірку всип приблизно на 1/4 її місткості калій перманганат КМnО4 і поклади біля отвору пробірки пухкий жмутик вати.
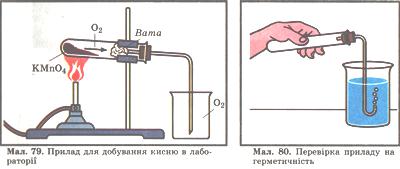
Закрий пробірку пробкою з газовідвідною трубкою. Закріпи пробірку в тримачі штатива так, щоб кінець газовідвідної трубки майже торкався дна стакана чи циліндра, в якому збиратиметься кисень.
Прогрій спочатку всю пробірку, а потім тільки ту частину, де міститься калій перманганат. Починай нагрівати пробірку з дна, потім переміщуй полум'я під ту частину, де калій перманганат ще не розклався. Досліди його властивості. Повноту заповнення стакана (циліндра) киснем перевіряй тліючою скіпкою. Як тільки посудина наповниться киснем, накрий її картоном або скляною пластинкою. Напиши рівняння реакцій: а) розкладу калій перманганату під дією нагрівання; б) взаємодії вуглецю з киснем (спалахування тліючої скіпки).
Подумай і спробуй відповісти (усно):
1. З якою метою біля пробки треба класти пухкий жмутик вати? 2. Чому вата не повинна торкатися калій перманганату? 3. На якій властивості кисню ґрунтується спосіб збирання його методом витіснення повітря? 4. Пригадай, який ти знаєш іще спосіб збирання кисню? Яку властивість кисню він засвідчує? 5. Якого типу реакція лежить в основі добування кисню в лабораторії? 6. Зроби висновок про фізичні й хімічні властивості кисню.
Хімія 7. Підручник для загальноосвітніх навчальних закладів. Н. М. Буринська
Оцініть статтю: 



